Водяной пар — это вода в газе. Газовые состояния относятся к трем основным кумулятивным состояниям воды, встречающимся в природе. Чистый водяной пар бесцветен и безвкусен. Наибольшее накопление водяного пара происходит в тропосфере.
Свойства паров в физике — формулы и определения с примерами
Туман является одним из наиболее часто наблюдаемых природных явлений в сельских и городских районах.
Испарение. Жидкости (и твердые тела) при любой температуре имеют много молекул (или атомов), кинетическая энергия которых больше их потенциальной энергии взаимодействия с соседними молекулами. Когда такие молекулы находятся вблизи поверхности жидкости, они легко покидают поверхность и образуют на ней пар.
Испарение — это процесс перехода вещества из влажного состояния в газообразное. Образование паров может происходить двумя способами: испарение и кипение.
Испарение — это испарение, происходящее с открытой поверхности жидкости при любой температуре.
Кипение — это образование пара, которое происходит по всему объему жидкости при определенной температуре.
Во время испарения частицы с высокой кинетической энергией покидают поверхность жидкости. В результате средняя кинетическая энергия других частиц жидкости уменьшается. Поэтому наблюдается жидкостное охлаждение (только если жидкость не переносит тепло извне).
Скорость испарения определяется. Температура жидкости, свободная поверхность жидкости, поток воздуха, окружающий поверхность жидкости, давление, приложенное к поверхности жидкости (из-за снижения давления, которое уменьшает скорость испарения) ), специальная теплота отвода жидкости, т.е. от типа жидкости.
Специальная теплота парообразования численно равна теплоте, необходимой для превращения 1 кг массы жидкости в пар при постоянной температуре.
Где
Единицы измерения теплоты образования специальных паров в СИ:.

Значение специальной парообразующей теплоты зависит от типа жидкости и ее температуры — значение специальной парообразующей теплоты уменьшается с повышением температуры. Минимальное значение специальной теплоты парообразования соответствует температуре кипения жидкости.
Теплота образования — это количество тепла, необходимое для преобразования массы жидкости в пар при определенной температуре.

Обратный процесс образования пара — это один из природных процессов, называемый конденсацией, при котором пар превращается в жидкость.
Концентрирование — это процесс преобразования пара в жидкость. Концентрированный пар передает тепло окружающей среде.
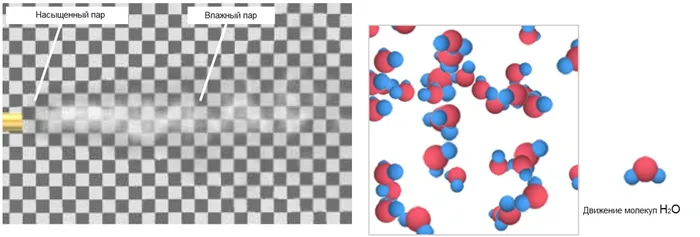
Насыщенный и ненасыщенный пар
Пары могут быть насыщенными или ненасыщенными, в зависимости от зависимости плотности и давления от температуры.
Насыщенные пары — это пары, находящиеся в динамическом равновесии с жидкостью. Динамическое равновесие между жидкостью и ее паром возникает, когда число молекул, покидающих свободную поверхность жидкости, равно числу молекул, возвращающихся в жидкость. Насыщенный пар появляется над свободной поверхностью жидкости в закрытом контейнере.
Если контейнер открыт, часть молекул, покидающих поверхность жидкости, испаряется в атмосферу и не возвращается в жидкость, т.е. динамическое равновесие нарушается, и пар становится ненасыщенным.
Ненасыщенный пар — это пар, который не находится в динамическом равновесии с жидкостью.
Свойства насыщенного пара
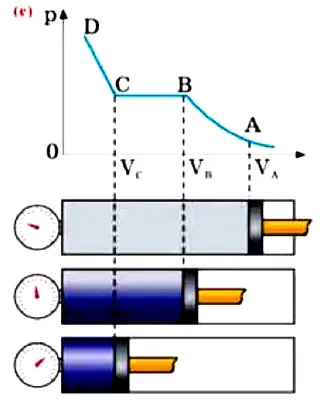
(a) Давление, плотность и концентрация насыщенного пара при постоянной температуре не зависят от количества пара. Другими словами, насыщенный пар не подчиняется принципу Бойля-Мариотта (a).
(b) При повышении температуры давление, плотность и концентрация насыщенного пара быстро увеличиваются. Другими словами, насыщенный пар не подчиняется закону Шарля. Это происходит потому, что увеличение давления насыщенных паров происходит в соответствии с уравнением (b).
Пар образуется молекулами воды при естественном испарении с поверхностей или при принудительном нагреве и кипении в водонагревательных баках. Помимо вышеупомянутых процессов, выделяется образование пара при сублимации льда. Однако это не имеет никакого отношения к плаванию.
Парообразование
Таким образом, испарение — это переход из жидкого состояния в газообразное.
Во время испарения энергия постоянно поглощается. Чтобы испариться, к веществу необходимо подвести тепло. Это увеличивает внутреннюю энергию вещества.
Существует два вида испарения: выпаривание и кипение.
Испарение — это превращение или переход жидкости с ее свободной поверхности в газ (пар). Если поверхность жидкости открыта и начинается переход вещества из жидкости в газ, это называется испарением.
Кипение — это процесс интенсивного парообразования, который происходит в жидкостях при определенных температурах.
Например, мы приготовили горячий чай. Вы можете видеть пар на вершине чашки, потому что вода только что вступила в процесс кипения.
В течение 30 минут мы не говорили, что кипение отличается от испарения. Это, конечно, верно, но оба процесса могут происходить параллельно.
Испарение может происходить без кипения, но мы его не ощущаем. Например, вода в озере испаряется, хотя мы этого не замечаем. Кипение — это, по сути, бурное испарение, вызванное внешними условиями, доводящее вещество до температуры кипения.
Физика объясняет испарение тем, что жидкости обычно немного холоднее окружающего воздуха, и испарение происходит из-за разницы температур.
В отсутствие внешних воздействий испарение жидкостей происходит очень медленно. Молекулы покидают жидкость благодаря эффекту диффузии.
Направление теплового потока при испарении может иметь различные порядки и комбинации.
Из глубины жидкости на поверхность, а затем в воздух, из
От жидкости, находящейся только на поверхности, до
на поверхность одновременно, водной и газообразной средой; и
только из воздуха на поверхность.
Подводя итог, чтобы избежать путаницы, скажите, каковы основные различия между испарением и кипячением?
При определенных температурах.
Температура кипения
При температуре кипения давление насыщенного пара равно внешнему давлению жидкости. Обычно это атмосферное давление. Поэтому, чем выше внешнее давление, тем выше температура, при которой начинается кипение.
При нормальном атмосферном давлении около 100 кПа температура кипения воды составляет 100 °C. Поэтому мы сразу можем сказать, что давление насыщенного водяного пара при температуре 100 градусов Цельсия составляет 100 кПа. Это значение полезно при поиске и устранении неисправностей.
Чем выше вы поднимаетесь, тем ниже становится атмосферное давление, поскольку масса атмосферы над вами уменьшается. Например, на вершине Эльбруса атмосферное давление составляет 5 x 104 Па, что вдвое меньше нормального атмосферного давления. Поэтому температура кипения на вершине Эльбруса также ниже, чем на уровне моря. Вода там закипает при температуре 82°C.
Температура кипения при нормальном атмосферном давлении является строго определенным значением для каждой жидкости.
Испарение и конденсация
Молекулы в жидкостях находятся в постоянном движении и хаосе. Это означает, что направление движения отдельных молекул является случайным. В то же время жидкость сохраняет свой объем. Кроме того, молекулы притягиваются друг к другу и не могут покинуть друг другаОмск. Жидкость.
Значения скорости молекул случайны. По этой причине можно с уверенностью сказать, что некоторые из всех молекул движутся очень быстро. Когда такие молекулы приближаются к границе раздела между жидкостью и окружающей средой, их кинетическая энергия может достигать высоких значений, и молекулы покидают жидкость.
Фактически, именно так происходит процесс испарения (как объяснялось выше при обсуждении фазовых переходов). По мере увеличения числа молекул, которые испаряются, образуется пар.
Возможен и обратный процесс. Молекулы, которые выходят из жидкости, возвращаются в жидкость. Это конденсация, о которой мы также говорили. Когда емкость с жидкостью открывают, испаряющиеся молекулы покидают пространство над жидкостью и не возвращаются обратно. Это уменьшает количество жидкости. Другими словами, жидкость испаряется, но пар не конденсируется (потому что молекулы пара удаляются из жидкости). Так происходит сушка.
Испарение может происходить с разной скоростью. Чем сильнее притяжение между молекулами, тем медленнее скорость испарения, так как меньшее количество молекул в единицу времени может преодолеть силу притяжения и улетучиться.
Такие жидкости, как эфир, ацетон и спирт, быстро испаряются. Из-за этого свойства их иногда называют летучими жидкостями. Вода испаряется медленнее. Масло и ртуть испаряются медленнее, чем вода.
Курсы подготовки к GCSE по физике могут помочь снизить стресс перед экзаменом и получить более высокие баллы.
(a) Давление, плотность и концентрация насыщенного пара при постоянной температуре не зависят от количества пара. Другими словами, насыщенный пар не подчиняется принципу Бойля-Мариотта (a).
Отличия
У них есть два отличия.
Насыщенные пары характеризуются термодинамическим равновесием. То есть, он имеет такое же давление и плотность, как и жидкость в закрытом контейнере.
По своим физическим свойствам насыщение близко к свойствам «идеального газа».
Таблица различий между насыщенным паром и водяным паром:.
| Свойства | Водяной | Насыщенный |
| Равновесие с жидкостью | Нет | Есть |
| Количество жидкости в сосуде | Становится меньше до полного испарения | Количество жидкости остается неизменным |
| Плотность | Низкая | Высокая |
| Изменение давления при повышении температуры | Не происходит | Повышается |
Различия между перегретым и насыщенным
Список основных различий:.
- Перегретый отличается от насыщенного большей температурой. В процессе его образования давление и температура не зависят друг от друга, что позволяет изменять эти значения для достижения большей эффективности для работы оборудования с паром 100% сухости.
- Вторая отличительная особенность – у перегретого больший удельный объем. Увеличенный объем газообразного вещества позволяет более эффективно его использовать и увеличивать производительность.
- Третье отличие характеризуется отсутствием конденсации. Постоянное подогревание создает условие, при котором к молекулам пара не присоединяются частицы воды. Процесс конденсации образуется после снижения температуры до значений характерных для образования насыщенного вещества.
Объединив различия между двумя парообразными состояниями, можно сделать вывод, что в перегретом состоянии вещество может повысить эффективность различных циклов производства тепла. Для достижения перегретого состояния используются дополнительные устройства.
Как происходит переход из одного состояния в другое?
Переход от насыщенных условий к перегретым происходит путем повышения температуры в замкнутом пространстве выше точки кипения. Важно отметить, что давление не изменяется во время перехода.
Процесс перехода водяного пара из одного состояния в другое очевиден при работе паровых котлов. Благодаря сгоранию топлива устройство работает при постоянной высокой температуре.

В его структуре происходят основные этапы парообразования.
- нагревание жидкости в котле до момента образования насыщения;
- образование газообразного соединения;
- подогрев до момента перехода из насыщенного состояния к перегретому.
В закрытом резервуаре содержится очищенная вода. Когда котел активируется, жидкость внутри него начинает нагреваться. Тепло влияет на активность молекул, которые начинают активно двигаться из-за возросшей кинетической энергии.
Молекулы быстро движутся и начинают уходить с поверхности воды в воздух, образуется пар, и постепенно объем закрытой емкости заполняется все еще активно движущимися молекулами. Пока объем емкости не заполнится полностью, это называется насыщением.
Если свободного пространства для движения недостаточно, давление и плотность частиц увеличиваются, и происходит конденсация. Взвешенные молекулы начинают возвращаться в жидкость.
Их количество равно количеству, выходящему из него, а давление остается постоянным. В этот момент в жидкости достигается равновесие, а пар становится насыщенным.
После процесса насыщения вещество может перейти к новой стадии — перегреву. Насыщенный газ проходит через специальное оборудование — нагревательный агент, который поддерживает температуру выше точки кипения.
Согревающая терапия запускает процесс испарения, и насыщенный пар перегревается. Газовые условия характеризуются большей и меньшей плотностью.
На практике даже самые лучшие котлы производят пар с содержанием влаги от 3% до 5%. При производстве пара присутствует некоторое количество воды, обычно в виде тумана или капель.
Пар как источник тепла
В настоящее время пар наиболее известен благодаря своему использованию в отоплении в качестве источника прямого и косвенного нагрева.
Прямой обогрев пáром
Методы прямого парового нагрева относятся к методам, при которых пар находится в непосредственном контакте с нагреваемым продуктом.
Следующий пример показывает, как китайские макароны готовятся на пару. Паровую корзину помещают в кастрюлю с кипящей водой. Пока вода кипит, пар поднимается в корзину и готовит пищу. В таких устройствах котел (сосуд) и паровой сосуд (корзина) объединены.
Принцип приготовления пищи на пару заключается в том, что пар вступает в непосредственный контакт с продуктами, так что скрытое тепло пара передается непосредственно продуктам и каплям воды, образующимся в результате конденсации.
В промышленности методы нагрева паром часто используются для приготовления пищи, стерилизации, пропаривания, вулканизации и других процессов.
Косвенный обогрев пáром
Косвенные методы парового нагрева относятся к процессам, в которых пар не вступает в прямой контакт с нагреваемым продуктом. Он широко используется в промышленности, поскольку обеспечивает быстрый и равномерный нагрев. Этот метод часто используется в теплообменниках для нагрева продуктов.
Преимущество этого метода перед непосредственным нагревом заключается в том, что капли воды, образующиеся при нагреве, не влияют на продукт. Поэтому пар можно использовать для различных процессов, таких как плавление, сушка и кипячение.
Непрямой нагрев паром используется в различных процессах, таких как производство продуктов питания и напитков, шин, бумаги, картона, топлива (например, бензина) и фармацевтических препаратов.
Подробнее о внедрении Steam в промышленность вы можете прочитать в следующих статьях на эту тему